| 铵 | |||
|---|---|---|---|
| |||
| |||
| 系统名 Ammonium | |||
| 识别 | |||
| CAS号 | 14798-03-9 | ||
| PubChem | 16741146 | ||
| ChemSpider | 218 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | QGZKDVFQNNGYKY-IKLDFBCSAZ | ||
| ChEBI | CHEBI:28938 | ||
| MeSH | D000644 | ||
| 性质 | |||
| 化学式 | H4N | ||
| 摩尔质量 | 18.04 g·mol−1 | ||
| pKa | 9.25 | ||
| 结构 | |||
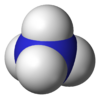
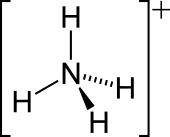
| 分子构型 | 正四面体 | ||
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |||

铵(拼音:ǎn,注音:ㄢ,英语:Ammonium,旧译作铔,化学式NH+4),又叫铵离子、铵根、铵根离子,是由氨分子衍生出的正一价、带1个正电的离子。氨分子与一个氢正离子配位结合就形成铵根离子(氨提供孤电子对)。铵离子在化学反应中相当于金属离子。
结构
存在

酸性环境下,溶解在水中的氨分子以铵根离子的形式存在。氨水可电离出铵根离子和氢氧根离子,浓氨水容易挥发为氨气。液氨自耦电离能产生铵离子。
铵盐
铵根离子还可以和阴离子结合形成盐,大部分铵盐都可溶。常见的铵盐有氯化铵、硝酸铵、硫酸铵、碳酸氢铵等。
命名
由于NH+4的化学性质类似于金属离子,故命名为金部的“铵”。
“铵”在中国内地的普通话拼音为“ǎ”,区别于阴平(第1声)的“氨”和去声(第4声)的“胺”。但在台湾地区,“铵”和“氨”读音均为“ān”。
一般的铵盐命名和普通的盐的命名一样,为某化铵或某酸铵,如氯化铵、醋酸铵等。
用途
用于铵盐中含氮,盐可用作氮肥,称为“铵态氮肥”。此类肥料不宜与碱性肥料混用,否则铵离子会被反应掉从而肥效降低。
常见的铵态氮肥有硫铵(硫酸铵)、碳铵(碳酸铵)、硝铵(硝酸铵)。
检验
铵盐的检验方法通常是与碱混合(必要时加热),会放出氨气。例如:
原理是铵盐与碱发生复分解反应,生成新盐和一水合氨,一水合氨易挥发为氨气和水。
铵盐可以与奈斯勒试剂反应生成黄棕色沉淀,用于定性检验。
衍生物
铵金属
在高压下,浸在大量自由电子海中的铵离子可能会表现出类似于金属的性质。冰巨星天王星与海王星的内部就可能存在这种“铵金属”。[1][2]
注解
- ↑ Stevenson, D. J. Does metallic ammonium exist?. Nature (Nature Publishing Group). 1975-11-20, 258: 222–223 [2012-01-13]. Bibcode:1975Natur.258..222S. doi:10.1038/258222a0.
- ↑ Bernal, M. J. M.; Massey, H. S. W. Metallic Ammonium (PDF). Monthly Notices of the Royal Astronomical Society (Wiley-Blackwell for the Royal Astronomical Society). 1954-02-03, 114: 172–179 [2012-01-13]. Bibcode:1954MNRAS.114..172B.