| 氨 | |
|---|---|
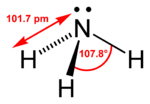
| |

| |
| IUPAC名 Ammonia [1] | |
| 系统名 Azane | |
| 别名 | 氮烷、阿摩尼亚 |
| 识别 | |
| CAS号 | 7664-41-7 |
| PubChem | 222 |
| ChemSpider | 217 |
| SMILES |
|
| InChI |
|
| InChIKey | QGZKDVFQNNGYKY-UHFFFAOYAF |
| Beilstein | 3587154 |
| Gmelin | 79 |
| 3DMet | B00004 |
| UN编号 | 1005 |
| EINECS | 231-635-3 |
| ChEBI | 16134 |
| RTECS | BO0875000 |
| KEGG | D02916 |
| MeSH | Ammonia |
| 性质 | |
| 化学式 | NH3 |
| 摩尔质量 | 17.0306 g·mol⁻¹ |
| 外观 | 具有非常刺鼻的气味的无色气体 |
| 密度 | 0.86 kg/m3 (1.013 bar ,沸点) 0.769 kg/m3 (STP)[2] |
| 熔点 | −77.73 °C(−107.91 °F;195.42 K)[5] |
| 沸点 | −33.34 °C(−28.01 °F;239.81 K)[5] |
| 溶解性(水) | 1:700 (0℃,100kPa) |
| 溶解性 | 可溶于氯仿、乙醚、乙醇和甲醇 |
| pKa | 32.5 (−33℃),[6] 10.5 (DMSO) |
| pKb | 4.75 (与水反应)[5] |
| 黏度 |
|
| 结构 | |
| 分子构型 | 三角锥 |
| 偶极矩 | 1.42 D |
| 热力学 | |
| ΔfHm |
−46 kJ·mol−1[8] |
| S |
193 J·mol−1·K−1[8] |
| 危险性 | |
GHS危险性符号   [9] [9]
| |
| GHS提示词 | Danger |
| H-术语 | H290, H301, H311, H314, H330, H334, H336, H360, H362, H373, H400 |
| P-术语 | P202, P221, P233, P261, P263, P271, P273, P280, P305+351+338, P310[9] |
| NFPA 704 | |
| 爆炸极限 | 15–28% |
| PEL | 50 ppm (25 ppm ACGIH- TLV; 35 ppm STEL) |
| 致死量或浓度: | |
LD50(中位剂量)
|
0.015 mL/kg (人类口服) |
LC50(中位浓度)
|
40,300 ppm (大鼠, 10 min) 28,595 ppm (大鼠, 20 min) 20,300 ppm (大鼠, 40 min) 11,590 ppm (大鼠, 1 hr) 7338 ppm (大鼠, 1 hr) 4837 ppm (小鼠。 1 hr) 9859 ppm (兔子, 1 hr) 9859 ppm (猫, 1 hr) 2000 ppm (小鼠, 4 hr) 4230 ppm (小鼠, 1 hr)[10] |
LCLo(最低)
|
5000 ppm (哺乳动物, 5 min) 5000 ppm (人类, 5 min)[10] |
| 相关物质 | |
| 其他阴离子 | 一水合氨 (NH3H2O) |
| 其他阳离子 | 铵 (NH4+) |
| 相关氢化物 | 氯化铵 (NH4Cl)、磷化氢、砷化氢、锑化氢、铋化氢 |
| 相关化学品 | 肼、叠氮酸、盐酸羟胺、氯胺 |
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |
氨[11](英语:Ammonia,或称氨气、无水氨,曾音译作𠼞、氩、阿摩尼亚,分子式为NH3)是无色气体,有强烈刺激气味(尿味),极易溶于水。常温常压下,1单位体积水可溶解700倍体积的氨。[5]氨对地球上的生物相当重要,是所有食物和肥料的重要成分。氨也是很多药物和商业清洁用品直接或间接的组成部分,具有腐蚀性等危险性质。
由于氨有广泛的用途,成为世界上产量最多的无机化合物之一,约八成用于制作化肥。2006年,氨的全球产量估计为1.465亿吨,主要用于制造商业清洁产品。
制法
固体铵盐制取
加热固体铵盐和碱的混合物 反应原理:
反应装置:固体+固体加热制气体装置。包括试管、酒精灯、铁架台(带铁夹)等。
净化装置(可省略):用碱石灰干燥。
收集装置: 向下排空气法,验满方法是用湿润的红色石蕊试纸置于试管口,试纸变蓝色;或将蘸有浓盐酸的玻璃棒置于试管口,有白烟产生。
尾气装置:收集时,一般在管口塞一团棉花球,可减少NH3与空气的对流速度,收集到纯净的NH3。
注意事项:不能用NH4NO3跟Ca(OH)2反应制氨气。硝酸铵受撞击、加热易爆炸,且产物与温度有关,可能产生NH3、N2、N2O、NO。
实验室制NH3不能用NaOH、KOH代替Ca(OH)2。因为NaOH、KOH是强碱,具有吸湿性(潮解)易结块,不易与铵盐混合充分接触反应。又KOH、NaOH具有强腐蚀性在加热情况下,对玻璃仪器有腐蚀作用,所以不用NaOH、KOH代替Ca(OH)2制NH3。
用试管收集氨气要堵棉花。因为NH3分子微粒直径小,易与空气发生对流,堵棉花目的是防止NH3与空气对流,确保收集纯净;减少NH3对空气的污染。
实验室制NH3除水蒸气用碱石灰,而不采用浓H2SO4和固体CaCl2。因为浓H2SO4与NH3反应生成(NH4)2SO4。NH3与CaCl2反应能生成CaCl2·8NH3(八氨合氯化钙)。
氮化物制法
可以用氮化物与水反应或者叠氮化物分解。如:
浓氨水制取
反应原理:。这种方法一般用于实验室快速制氨气。
装置:烧瓶,酒精灯,铁架台,橡胶塞,导管等。
注意事项:加热浓氨水时也会有水蒸气,需要用干燥装置除杂。同上,这种方法制NH3除水蒸气用碱石灰,而不要采用浓H2SO4和固体CaCl2。[12]
浓氨水中存在以下平衡:
NH3+H2O ⇌ NH3·H2O ⇌NH4+ +OH-
加入固态碱性物质(如CaO,NaOH,碱石灰等),消耗水且使OH-的数量增加,使平衡往中间移动,同时反应放热,促使NH3·H2O的分解。
工业合成氨
合成氨指由氢气、氮气在高压、高温、催化剂作用下直接化合生成的氨,是固氮的一种方法。目前世界上的氨,除少数从焦炉气中回收的副产品外,绝大部分均由合成法制造。反应必须通过使用催化剂完成。
测试
由于氨是弱碱性,所以用红色石蕊纸测试氨,会呈蓝色。由于氨气是气体,所以要先浸湿试纸。
氨水
氨水(NH3(aq),也常写成 NH4OH)又称为阿摩尼亚水,指氨的水溶液,有强烈刺鼻气味,具弱碱性。
氨水中,氨气分子发生微弱水解生成氢氧根离子及铵根离子。“氢氧化铵”事实上并不存在,只是对氨水溶液中的离子的描述,并无法从溶液中分离出来。
氨的在水中的电离可以表示为:
反应平衡常数。
1M氨水的pH值为11.63,大约有0.42%的NH3变为NH+4。
氨水是实验室中氨的常用来源。它可与含铜(II)离子的溶液作用生成深蓝色的配合物,也可用于配置银氨溶液等分析化学试剂。
用途
- 氨水可被土中的土壤胶体吸附和被作物吸收,无残留物质,适用于各种土壤和作物。
- 由于氨拥有强烈的刺激性气味,在医疗方面,会用少量易于挥发的氨作为使人清醒的吸入剂。
- 生产硝酸
- 玻璃清洁剂
- 有八成的氨生产氮肥
- 航空燃料(X-15)
- 氨是最广泛用的制冷剂之一,可用于空调、冷藏和低温,能用于各种形式的制冷压缩机,蒸发温度可控制在5度至零下65度,代号R717。
反应
络合反应
NH3分子中氮原子有一对孤对电子,可以作为电子对给予体(路易斯碱)形成加合物。如氨在氢离子络合生成铵离子:
NH3亦可与金属离子如Ag+、Cu2+等发生错合,生成错合物:
氧化还原
NH3分子中氮为-3价,在适当条件下可被氧化为N2或更高价氮化合物。
如NH3在纯氧中燃烧,生成N2:
在铂催化下可氧化生成水与一氧化氮,是工业制硝酸的重要反应。
可还原CuO为Cu:
常温下NH3可与强氧化剂(如氯气、过氧化氢、高锰酸钾)直接反应:
酸碱中和
氨与强酸反应,生成的盐大多为弱酸性。氨与弱酸(如乙酸)反应,盐则为中性。
酸碱中和是放热反应。
有机反应
氨分子的氮上有一对孤对电子,而且带部分负电荷,因此氨具有亲核性。换言之,氨是个亲核试剂,因此可与亲电体反应。
例如,氨与卤代烃发生双分子亲核取代反应生成胺。该反应又称氨解反应。
液氨
液氨(NH3)指的是液态的氨,为工业上氨气的主要储存形式。是一种常用的非水溶剂和制冷剂,也是除了水以外最常用的无机溶剂。不过由于它的挥发性和腐蚀性,液氨在储存和运输时发生事故的机率也相当高。
备注
- ↑ NOMENCLATURE OF INORGANIC CHEMISTRY IUPAC Recommendations 2005 (PDF).
- ↑ Gases – Densities. [3 March 2016].
- ↑ Yost, Don M. Ammonia and Liquid Ammonia Solutions. Systematic Inorganic Chemistry. READ BOOKS. 2007: 132. ISBN 978-1-4067-7302-6. 已忽略文本“chapter-” (帮助)
- ↑ Blum, Alexander. On crystalline character of transparent solid ammonia. Radiation Effects and Defects in Solids. 1975, 24 (4): 277. doi:10.1080/00337577508240819.
- ↑ 5.0 5.1 5.2 5.3 氨;氨气;ammonia. 化工引擎. [2008-05-06].
- ↑ Perrin, D. D., Ionisation Constants of Inorganic Acids and Bases in Aqueous Solution; 2nd Ed., Pergamon Press: Oxford, 1982.
- ↑ Iwasaki, Hiroji; Takahashi, Mitsuo. Studies on the transport properties of fluids at high pressure. The Review of Physical Chemistry of Japan. 1968, 38 (1).
- ↑ 8.0 8.1 Zumdahl, Steven S. Chemical Principles 6th Ed.. Houghton Mifflin Company. 2009: A22. ISBN 978-0-618-94690-7.
- ↑ 9.0 9.1 来源:Sigma-Aldrich Co., Ammonia (20 July 2013查阅).
- ↑ 10.0 10.1 Ammonia. Immediately Dangerous to Life and Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ↑ (拼音:ān)拼音:ān,注音:ㄢ,音同“安”
- ↑ 实验室如何制取氨气 有什么其它制作方法呢_氨气的预防方法_氨气制法的其它方法_健康资讯_快速问医生. m.120ask.com. [2021-01-07].
