| 二氧化鈦 | |
|---|---|

| |
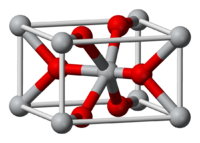
| |
| IUPAC名 Titanium dioxide Titanium(IV) oxide | |
| 識別 | |
| CAS號 | 13463-67-7 |
| PubChem | 26042 |
| ChemSpider | 24256 |
| SMILES |
|
| InChI |
|
| InChIKey | GWEVSGVZZGPLCZ-TYTSCOISAW |
| ChEBI | 32234 |
| RTECS | XR2775000 |
| KEGG | C13409 |
| 性質 | |
| 化學式 | TiO2 |
| 摩爾質量 | 79.87 g·mol⁻¹ |
| 外觀 | 白色固體 |
| 密度 | 4.23 |
| 熔點 | 1870 °C (3398 °F) |
| 沸點 | 2972 °C (5381.6 °F) |
| 溶解性(其他溶劑) | 不可溶 |
| 熱力學 | |
| ΔfHm |
−945 kJ/mol[1] |
| 危險性 | |
| 歐盟分類 | 未列明 |
| NFPA 704 | |
| 閃點 | 不可燃 |
| 相關物質 | |
| 其他陽離子 | 一氧化鈦 三氧化二鈦 三氧化五鈦 二氧化鋯 二氧化鉿 |
| 若非註明,所有數據均出自一般條件(25 ℃,100 kPa)下。 | |
二氧化鈦,化學式為TiO2,俗稱鈦白粉,分子大小是奈米級為光觸媒,能靠紫外線消毒及殺菌,已經有一些產品問世。 亦可用於化妝品中。 二氧化鈦是水反應生成氫氣和氧氣的催化劑, 二氧化鈦可製作成光催化劑,淨化空氣,消除車輛排放物中25%到45%的氮氧化物,可用於治理PM2.5懸浮顆粒物過高的空氣污染。
存在形式
| 形式 | 晶系 | 合成 |
|---|---|---|
| 金紅石 | 四方晶系 | |
| 銳鈦礦 | 四方晶系 | |
| 板鈦礦 | 斜方晶系 | |
| TiO2(B)[2] | 單斜晶系 | Hydrolysis of K2Ti4O9 followed by heating |
| TiO2(H), hollandite-like form[3] | 四方晶系 | Oxidation of the related potassium titanate bronze, K0.25TiO2 |
| TiO2(R), ramsdellite-like form[4] | 斜方晶系 | Oxidation of the related lithium titanate bronze Li0.5TiO2 |
| TiO2(II)-(α-PbO2-like form)[5] | 斜方晶系 | |
| baddeleyite-like form, (7 coordinated Ti)[6] | 單斜晶系 | |
| TiO2 -OI[7] | 斜方晶系 | |
| cubic form[8] | 立方晶系 | P > 40 GPa, T > 1600 °C |
| TiO2 -OII, cotunnite(PbCl2)-like[9] | 斜方晶系 | P > 40 GPa, T > 700 °C |
製備
鈦白粉的生產方法有硫酸法和氯化法兩種。硫酸法是將鈦鐵礦經濃硫酸酸解成塊狀固相物,用酸性水浸取後得到鈦液,經沉降除雜質、冷凍分離副產硫酸亞鐵後,加晶種使硫酸氧鈦分解生成偏鈦酸。經水洗達標後煅燒、粉碎而製得鈦白粉。
反應方程式:
H2SO4 + TiO2→TiOSO4 + H2O
Ti(SO4)2 + H2O→ TiOSO4 + H2SO4
TiOSO4 + H2O→H2TiO3↓+ H2SO4 H2TiO3·SO3→TiO2+H2O+SO3↑
氯化法是將粉碎後的金紅石或高鈦渣與焦炭混合,在硫化床氯化爐中與氯氣反應生成四氯化鈦,經淨化,加入晶型轉化劑於高濁罡氧化生成二氧化鈦,再經水洗、乾燥、粉碎得到。 反應方程式:
2TiO2 + 3C + 4Cl2→2TiCl4 + 2CO↑+ CO2↑
TiCl4(g)+O2 (g)→TiO2 (s)+ 2Cl2 (g)
用途
參考資料
- ↑ Zumdahl, Steven S. Chemical Principles 6th Ed.. Houghton Mifflin Company. 2009: A23. ISBN 0-618-94690-X (英語).
- ↑ Marchand R., Brohan L., Tournoux M. A new form of titanium dioxide and the potassium octatitanate K2Ti8O17. Materials Research Bulletin. 1980, 15 (8): 1129–1133. doi:10.1016/0025-5408(80)90076-8.
- ↑ Latroche, M; Brohan, L; Marchand, R; Tournoux,. New hollandite oxides: TiO2(H) and K0.06TiO2. Journal of Solid State Chemistry. 1989, 81 (1): 78–82. Bibcode:1989JSSCh..81...78L. doi:10.1016/0022-4596(89)90204-1.
- ↑ Akimoto, J.; Gotoh, Y.; Oosawa, Y.; Nonose, N.; Kumagai, T.; Aoki, K.; Takei, H. Topotactic Oxidation of Ramsdellite-Type Li0.5TiO2, a New Polymorph of Titanium Dioxide: TiO2(R). Journal of Solid State Chemistry. 1994, 113 (1): 27–36. Bibcode:1994JSSCh.113...27A. doi:10.1006/jssc.1994.1337.
- ↑ Simons, P. Y.; Dachille, F. The structure of TiO2II, a high-pressure phase of TiO2. Acta Crystallographica. 1967, 23 (2): 334–336. doi:10.1107/S0365110X67002713.
- ↑ Sato H. , Endo S, Sugiyama M, Kikegawa T, Shimomura O, Kusaba K. Baddeleyite-Type High-Pressure Phase of TiO2. Science. 1991, 251 (4995): 786–788. Bibcode:1991Sci...251..786S. PMID 17775458. doi:10.1126/science.251.4995.786.
- ↑ Dubrovinskaia N A, Dubrovinsky L S., Ahuja R, Prokopenko V B., Dmitriev V., Weber H.-P., Osorio-Guillen J. M., Johansson B. Experimental and Theoretical Identification of a New High-Pressure TiO2 Polymorph. Phys. Rev. Lett. 2001, 87 (27 Pt 1): 275501. Bibcode:2001PhRvL..87A5501D. PMID 11800890. doi:10.1103/PhysRevLett.87.275501.
- ↑ Mattesini M, de Almeida J. S., Dubrovinsky L., Dubrovinskaia L, Johansson B., Ahuja R. High-pressure and high-temperature synthesis of the cubic TiO2 polymorph. Phys. Rev. B. 2004, 70 (21): 212101. Bibcode:2004PhRvB..70u2101M. doi:10.1103/PhysRevB.70.212101.
- ↑ Dubrovinsky, LS; Dubrovinskaia, NA; Swamy, V; Muscat, J; Harrison, NM; Ahuja, R; Holm, B; Johansson, B. Materials science: The hardest known oxide. Nature. 2001, 410 (6829): 653–654. Bibcode:2001Natur.410..653D. PMID 11287944. doi:10.1038/35070650.
